سختی آب چیست؟ مقادیر کمی
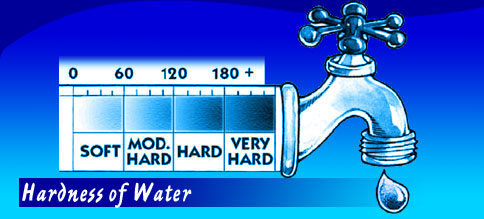
سختی آب که معمولا قابلیت آب در فعل و انفعال با صابون را تداعی میکند، به مجموعه املاح «کلسیم» و «منیزیم» موجود در آب که بر حسب میلیگرم در لیتر «کربنات کلسیم» بیان میشود، اطلاق میگردد.
سختی آب شاخص عناصر تشکل دهنده املاح محلول در آب نیست و فقط به برخی از آنیونها و کاتیونهای آب ارتباط دارد.
سختی آب در درجه اول به ترکیبات کلسیم و منیزیم و به میزان کمتری به سایر یونهای فلزی با ظرفیت بالا مانند سرب، استرنسیم، باریم و ... مربوط است.
سختی آب در سیستم متریک، بر حسب میلیگرم در لیتر کربنات کلسیم اندازهگیری میشود و در سایر سیستمهای اندازهگیری واحدهای دیگری دارد.
سختی آب، عملا شاخص میزان فعل و انفعال آب با صابون است و برای شستوشو با آبهای سختتر به صابون زیادتری نیاز است.
آبهای سخت در درجه حرارت بالا در جداره ظروف و در صنعت در دیگهای بخار، رسوبات کربنات کلسیم ایجاد میکنند.
تماس آب با ترکیبات آهکی موجود در سطح زمین یا تشکیلدهندههای قشر خاک باعث ورود عوامل سختی در آبها شده و معمولا آبهای زیرزمینی از سختی زیادتری نسبت به آبهای سطحی برخوردارند.
آبها را از نظر سختی بر حسب میلیگرم در لیتر کربنات کلسیم به ترتیب زیر طبقهبندی کردهاند.
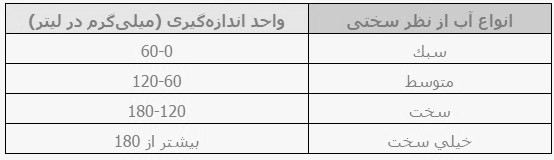
ترکیبات کلسیم به میزان کم در آب حل میشوند؛ اما وجود گازکربنیک در آب باعث افزایش حلالیت این ماده میشود. به یاد داشته باشید که مصرف مواد غذایی، باعث ورود مقادیر قابل توجهی کلسیم و منیزیم به بدن میشود. روزانه تا 1000 میلیگرم کلسیم و 200-400 میلیگرم منیزیم جذب بدن هر انسان بالغ میشود که منبع اصلی آن محصولات لبنی و مواد گوشتی است.تجربه نشان داده است که روزانه 35 درصد کلسیم و منیزیم مورد نیاز از طریق مصرف مواد غذایی، جذب بدن میشود.
عوارض مطلوب و نامطلوب مصرف آبهای سخت و سبک به دو گروه آثار شیمیایی و فیزیولوژیکی تقسیم میشوند.
از مهمترین آثار نامطلوب شیمیایی مصرف آبهای سخت، ایجاد رسوبات سخت کربنات کلسیم در کتری، سماور و دیگهای بخار تاسیسات حرارتی منازل که با آب در تماس هستند، است که باعث بروز خسارات فراوان میشود.
از جمله آثار فیزیولوژیک آبهای سخت میتوان به ترکیب منیزیم با یون سولفات و تشکیل سولفات منیزیم اشاره کرد که اثر مسهلی دارد. آبهای نرم با pHپایینتر تمایل زیادتری در انحلال املاح و فلزات موجود در شبکههای توزیع آب دارند، به همین دلیل در این گونه آبها همواره فلزاتی نظیر سرب، کادمیوم، روی و مس دیده میشود که مصرف مداوم آنها هر کدام با اثرات فیزیولوژیک خاصی در مصرف کننده همراه است. تجربه نشان داده است که وجود کلسیم با غلظت بالا در آبهای آشامیدنی مانع جذب این فلزات در بدن میشود. این عامل سبب جانشین شدن سرب در اعضای بدن، به خصوص استخوانها به جای کلسیم میشود.
بعضی دانشمندان معتقدند، بهتر است کلسیم و منیزیم لازم بدن توسط غذا تامین شود و حتیالامکان از آبهای سبک برای شرب استفاده شود. باید توجه داشت که بدن نسبت به سنگینی موجود در آب مورد مصرف خود حساسیت دارد، چنانچه این نوشیدنی تغییر یابد، ممکن است در دستگاه گوارش ایجاد اخلال نماید و این موضوع را به اصطلاح آب به آب شدن میگویند.
واحدهای بکار رفته در سختی آب
در صورتی که مقادیر کاتیونهای مختلف برحسب میلیگرم بر لیتر (ppm) در دست باشد، معمولا برای سهولت، به کمک فاکتورهایی که از تقسیم وزن مولکولی کربنات کلسیم به وزن اتمی هر یک از عناصر بدست آمده، این مقادیر برحسب کربنات کلسیم محاسبه و بیان میشود. سختی آب، معمولا بر حسب ppm یعنی mg/lit (میلیگرم بر لیتر) بیان میشود.
در بعضی از طبقهبندیها حداکثر سختی آبهای قابل شرب ، 300 میلیگرم در لیتر کربنات کلسیم تعیین شده است.
راه حل سختی زدایی آب شرب
یکی از روشهای سختیزدایی، استفاده از سامانههای تصفیه آب خانگی است که با قیمت ناچیزی میتوان آن را تهیه کرد. روش کار آنموئینگی معکوس یا همان اسمز معکوس (Reverse Osmosis) است. خروجی آب این دستگاهها در حد آب آشامیدنی استاندارد گزارش شده است

مدیر سایت: بهزاد سرهادی کارشناس ارشد مهندسی آب
شناسه تلگرام مدیر سایت: SubBasin@
نشانی ایمیل: behzadsarhadi@gmail.com
(سوالات تخصصی را در گروه تلگرام ارسال کنید)
_______________________________________________________
پروژه تخصصی در لینکدین







 در منابع آب
در منابع آب




















نظرات (۰)